Enunciado Completo:
- No modelo de Bohr para o átomo de hidrogênio (Cap. 2, Probl. 3), calcule:
(a) a razão da energia potencial eletrostática do elétron a sua energia cinética;
(b) a energia necessária para ionizar o átomo, em elétron-volts.
Resolução Passo a Passo:
No modelo de Bohr para o átomo de hidrogênio, um elétron de carga -e e massa m orbita um próton de carga +e em uma trajetória circular de raio r, sob a ação da força Coulombiana atrativa.
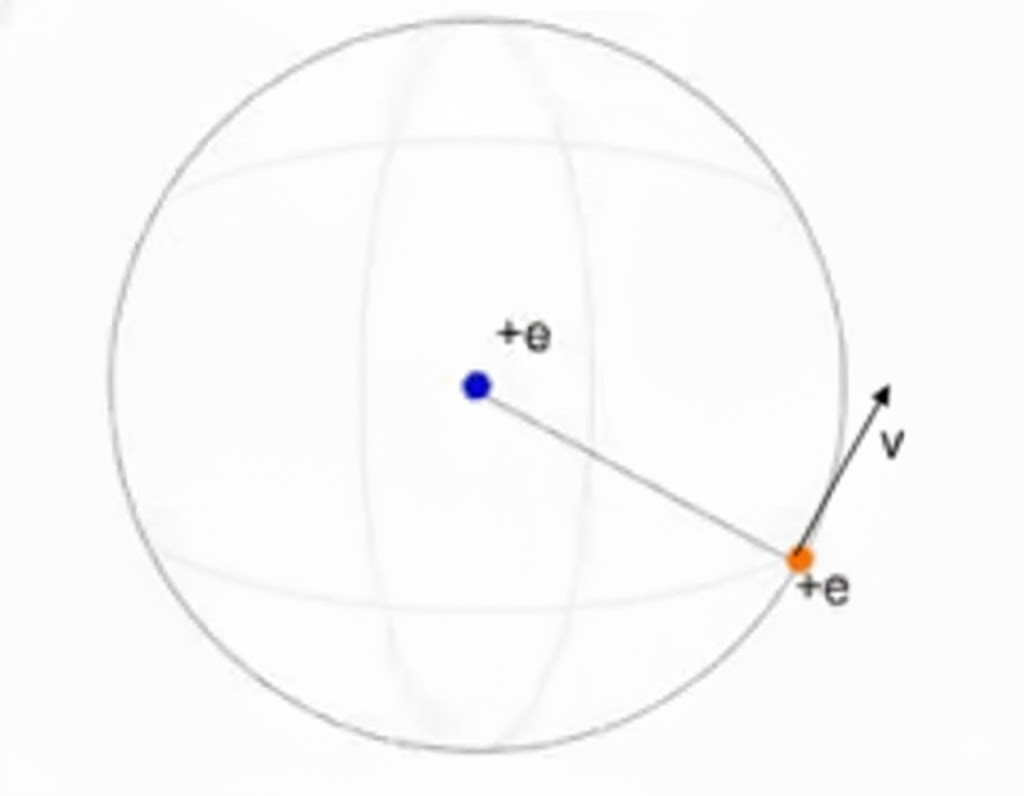
(a) Razão U/E_c
Passo 1: Força centrípeta.
A força de atração Coulombiana fornece a força centrípeta necessária para o movimento circular:
\dfrac{1}{4\pi\epsilon_0} \dfrac{e^2}{r^2} = m \dfrac{v^2}{r}
onde v é a velocidade orbital do elétron.
Passo 2: Energia cinética.
Da equação acima, multiplique ambos os lados por r/2:
\dfrac{1}{2} m v^2 = \dfrac{1}{2} \cdot \dfrac{1}{4\pi\epsilon_0} \dfrac{e^2}{r}
Portanto, a energia cinética é:
Passo 3: Energia potencial eletrostática.
U = \dfrac{1}{4\pi\epsilon_0} \dfrac{(+e)(-e)}{r} = -\dfrac{1}{4\pi\epsilon_0} \dfrac{e^2}{r}Passo 4: Razão.
\dfrac{U}{E_c} = \dfrac{-\dfrac{1}{4\pi\epsilon_0} \dfrac{e^2}{r}}{\dfrac{1}{8\pi\epsilon_0} \dfrac{e^2}{r}} = \dfrac{-1/4}{1/8} = -2Resposta (a): \dfrac{U}{E_c} = -2
(b) Energia de ionização
Passo 1: Energia total do elétron no estado ligado.
A energia total E é a soma da energia cinética e potencial:
Passo 2: Usar o raio da órbita fundamental de Bohr.
Bohr postulou que o momento angular é quantizado: m v r = n \hbar, com \hbar = h/(2\pi).
Para o estado fundamental (n=1), o raio é:
r_1 = a_0 = \dfrac{4\pi\epsilon_0 \hbar^2}{m e^2} = 5.29 \times 10^{-11} \, \text{m} (raio de Bohr).
Passo 3: Calcular a energia total no estado fundamental.
Substitua r = a_0 na expressão de E:
E_1 = -\dfrac{1}{8\pi\epsilon_0} \dfrac{e^2}{a_0}
Mas a_0 = \dfrac{4\pi\epsilon_0 \hbar^2}{m e^2}, então:
Passo 4: Expressar em termos de constantes fundamentais.
A energia de ionização E_{ion} é o mínimo trabalho necessário para remover o elétron do átomo, levando-o para o infinito com energia cinética zero. Isso corresponde a E_{ion} = -E_1 (pois a energia no infinito é zero por convenção).
O valor numérico é conhecido:
E_{ion} = \dfrac{m e^4}{32\pi^2\epsilon_0^2 \hbar^2} = \dfrac{e^2}{8\pi\epsilon_0 a_0}Passo 5: Calcular numericamente.
Use as constantes:
- \dfrac{e^2}{4\pi\epsilon_0} = 1.44 \, \text{eVnm} (pois e^2/(4\pi\epsilon_0) = 1.44 \times 10^{-9} \, \text{eVm})
- a_0 = 0.0529 \, \text{nm}
Então:
E_{ion} = \dfrac{1}{2} \cdot \dfrac{1}{4\pi\epsilon_0} \dfrac{e^2}{a_0} = \dfrac{1}{2} \times \dfrac{1.44 \, \text{eVnm}}{0.0529 \, \text{nm}}
Resposta (b): A energia de ionização do átomo de hidrogênio no modelo de Bohr é 13.6 \, \text{eV} (arredondando para uma casa decimal).
Resumo das Respostas Finais:
(a) \dfrac{U}{E_c} = -2
(b) E_{ion} \approx 13.6 \, \text{eV}

